Ley de los gases ideales
Un gas ideal es aquel cuyas moléculas no están sometidas a fuerzas internas de interacción (aunque no entraremos en detalle, según la 3ª ley de Newton, dos partículas se ejercen una fuerza la una a la otra de igual módulo y dirección pero sentido contrario; sin embargo esta fuerza de interacción es despreciable en los gases ideales). Además, en ellos los choques son elásticos (se conserva en ellos la energía y el momento lineal).
Los gases ideales cumplen la siguiente ecuación:

La constante los gases ideales es universal y tiene un valor:
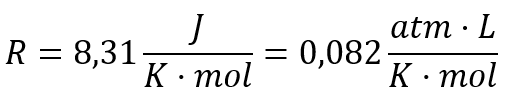
NOTA: Para el cambio de unidades se utiliza un factor de conversión.
NOTA: La temperatura siempre estará expresada en grados Kelvin (K). La presión, sin embargo, se puede expresar con diferentes unidades como pascales (Pa) o atmósferas (atm); aunque NUNCA se nos debe olvidar que debemos tener en cuenta que el valor de la constante universal debe tener dimensiones acordes a la unidad que hemos utilizado para la presión.
dependiendo de las unidades que utilicemos para la constante universal.
POR OTRA PARTE, debemos tener en cuenta (puede que nos encontremos ante un problema en el que no se nos especifique el volumen del gas ideal) que el volumen ocupado por un mol de gas ideal en condiciones normales de temperatura, 1 atm y 0º C (o en Kelvin, 273 K), es V=22,4 L.
En la siguiente tabla se muestra cuándo usar un valor de R u otro (son equivalentes siempre, sólo que con diferentes unidades).

Veamos un ejemplo:
EJEMPLO: Un gas ideal está a 15ºC. Teniendo en cuenta que el gas se encuentra a presión atmosférica (1 atm), ¿que volumen ocuparán 4 moles del gas?


SOLUCIÓN: El volumen que ocupará el gas será aproximadamente 94,46 L.
Aunque en la realidad, los gases SÍ tienen fuerzas internas internas de interacción, en ciertas condiciones (especialmente presiones bajas y temperaturas altas), estas son prácticamente despreciables y es válida la ecuación de los gases ideales.
Un gas ideal cumple 4 leyes o principios. Al combinar estos principios, se obtiene la ley de los gases ideales. En esta entrada, hemos escrito en primer lugar la ley de los gases ideales, pues a partir de ella se puede obtener los 4 principios citados, SIN EMBARGO, estos principios fueron descubiertos con anterioridad a la formulación de la ley de los gases ideales.
1. Ley de Boyle-Mariotte.
2. Ley de Charles.
3. Ley de Gay-Lussac.
4. Principio de Avogadro.
A continuación el test de autoevaluación. Mirar antes de realizarlo Ley de Boyle-Mariotte, Ley de Charles, Ley de Gay-Lussac y Principio de Avogadro:
Test de autoevaluación
* Para tomar nuevamente la autoevaluación presione el botón 'F5'
Test de autoevaluación resuelto aquí abajo:
